塩酸・砂糖水・アンモニア水とかって何性だったでしょうか。3つの性質に分けることができたと思います。
今回は、水溶液の性質について学習します。
〇酸・アルカリ
1.酸性の水溶液(~酸がつくものが多い)
特徴
①リトマス試験紙の色:青色→赤色
②水素を持つ:酸はその成分中に水素を持っている
③水素を発生:酸のうすい水溶液に亜鉛(鉄・マグネシウム・アルミニウム等)をつけると、気体の水素を発生
④伝導性:酸は水に溶けて、その溶液は電気を流す
⑤味:酸の薄い水溶液は酸味をもつ
⑥アルカリと反応すると、①~⑤の性質をほとんど失う
・塩酸 (気体:塩化水素)
特性:無色透明・特有な刺激臭・石灰石や炭酸ナトリウム、炭酸水素ナトリウムを加えると、二酸化炭素が発生する
亜鉛・鉄・アルミニウム・マグネシウム・ニッケル・スズなどに加えると、水素を発生する
・炭酸水(気体:二酸化炭素) 金属と反応して水素が発生。
・硫酸 亜鉛、鉄、マグネシウムと反応し水素が発生。
・酢 (液体:酢酸)
特性:無色透明・刺激臭が強い・亜鉛、鉄、マグネシウムと反応しゆっくり水素を発生」
2.アルカリ性の水溶液(水酸化~がつくものが多い)
※アルカリ性のものは、水に溶けやすい
・水酸化ナトリウム水溶液
・水酸化カリウム水溶液
・アンモニア水(気体:アンモニア)特有な刺激臭
・石灰水(固体:水酸化カルシウム)
3.中性の水溶液
・食塩水(固体:塩化ナトリウム=食塩)
・砂糖水
〇指示薬
\begin{array}{c|c|c|c}
\ & アルカリ性 & 中性 & 酸性 \\
\hline
リトマス紙 & 赤色→青色 & — & 青色→赤色 \\
\hline
BTB液 & 青色 & 緑色 & 黄色 \\
\hline
(二酸化炭素) & 少ない & ←→ & 多い \\
\hline
フェノールフタレイン溶液 & 赤色 & — & —
\end{array}
〇中和
中和…酸性とアルカリ性の水溶液を混ぜ合わせたときに起こる、互いの性質を打ち消しあう反応のこと。
例)塩酸に水酸化ナトリウムの水溶液を加えていく
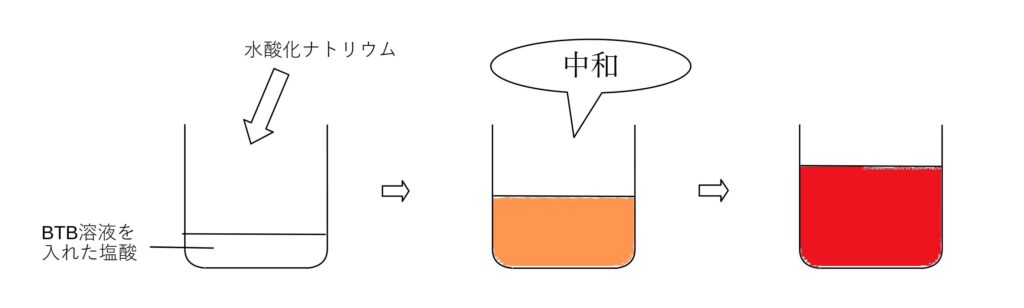
左から、酸性→中性→アルカリ性 となる
〇中性の時の反応
酸性+アルカリ性 → 塩(えん)+水 (中和)
他 硫酸+水酸化バリウム水溶液→硫酸バリウム+水
※硫酸バリウムは自己沈殿する
うすい塩酸+アンモニア水→塩化アンモニウム+水